EE UU aprueba el tratamiento con transfusiones de plasma para pacientes con coronavirus
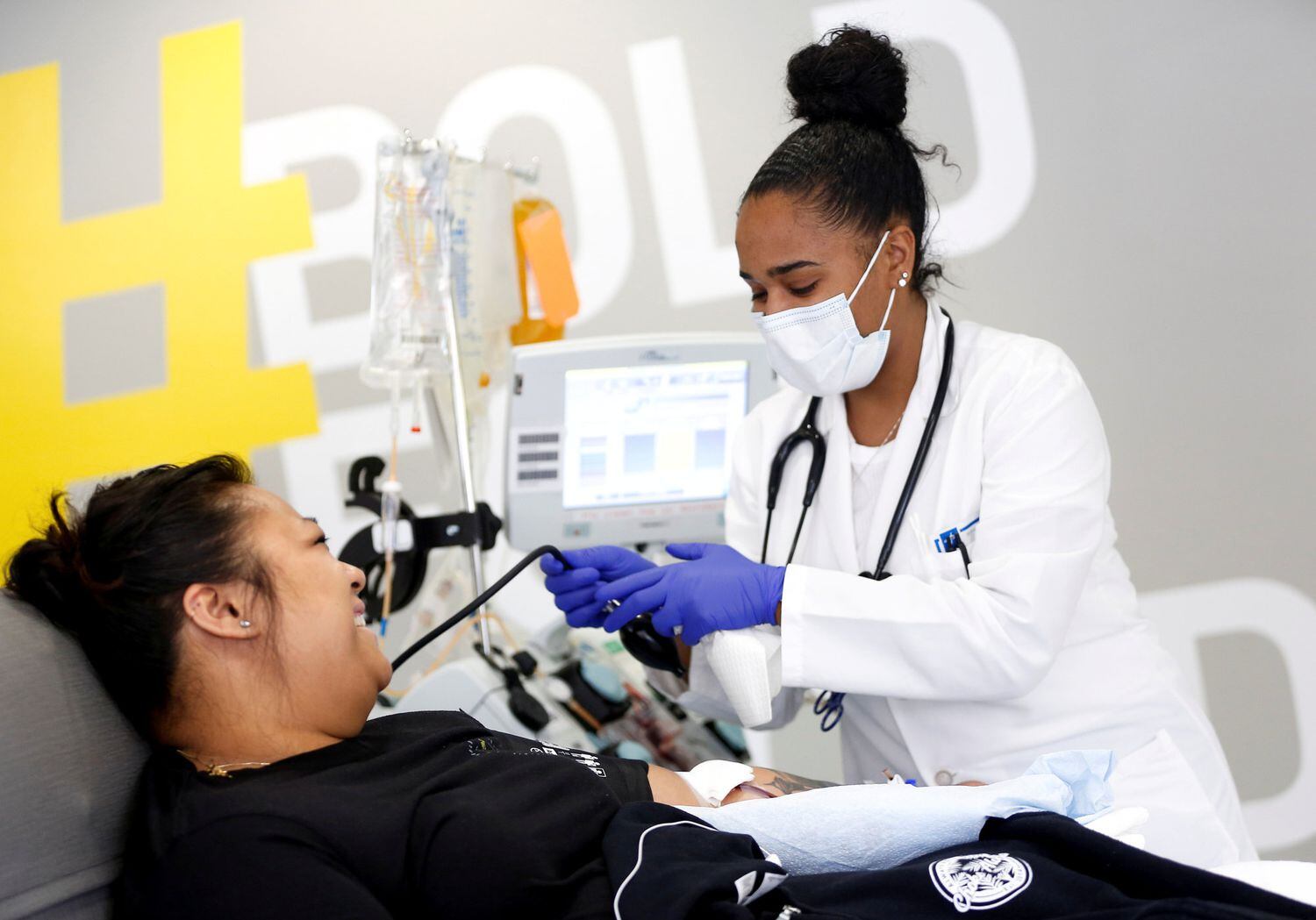
Una paciente dona plasma en una clínica en Seattle.
Los primeros estudios señalan que un 35% de los enfermos se recupera tras recibir el tratamiento.
WASHINGTON – La Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) ha autorizado de emergencia el uso de plasma como tratamiento para los pacientes con coronavirus. La agencia federal ha analizado en los últimos meses los resultados de enfermos que han recibido transfusiones del componente líquido de la sangre de pacientes que se han recuperado de la enfermedad. El plasma contiene un alto nivel de anticuerpos que, según los análisis de la agencia, ayudan a la recuperación del paciente en algunos casos.
La agencia había detenido la autorización la semana pasada asegurando que los resultados de las investigaciones no habían sido concluyentes. Este domingo, la FDA ha asegurado que analizó los resultados de 20.000 pacientes que recibieron transfusiones de plasma. Estos tenían menos de 80 años, habían sido hospitalizados y aún no utilizaban un ventilador como ayuda para respirar. La agencia señala que al menos un 35% de los enfermos tuvieron una recuperación favorable tras recibir el tratamiento. En Estados Unidos se estima que unas 70.000 personas con la covid-19 ya les ha sido administrada una transfusión de plasma de un paciente recuperado.
Este domingo, la FDA ha dado un rápido y súbito giro para permitir el uso del tratamiento. “Los estudios realizados este año muestran que el plasma de los pacientes que se han recuperado de la covid-19 tienen el potencial de ayudar a tratar a aquellos pacientes que están sufriendo por los efectos de este terrible virus”, explicó Stephen Hahn, comisionado de la FDA. Los estudios sobre el tratamiento todavía están en curso por lo que la agencia federal se ha comprometido a actualizar su autorización.
Hasta ahora el único tratamiento que había sido autorizado por la FDA era el antiviral experimental remdesivir, elaborado por la compañía farmacéutica Gilead, y que recibió luz verdad en Estados Unidos en mayo. El medicamento fue creado para tratar el ébola y la hepatitis, pero no dio resultados satisfactorios. Frente a la covid-19, el fármaco actúa como un bloqueador del virus cuando entra al cuerpo humano. Hasta ahora en Estados Unidos se han presentado 5,6 millones de casos y 176.000 personas han muerto por la enfermedad.
La última autorización ha sido anunciada este domingo por Donald Trump en la Casa Blanca. El presidente estadounidense había atacado esta semana en Twitter a la agencia por supuestamente impedir que la vacuna contra el coronavirus esté disponible para los estadounidenses antes del 3 de noviembre, el día de las elecciones presidenciales. “La FDA está haciendo muy difícil que las compañías farmacéuticas lleguen a la gente para hacer las pruebas con las vacunas”, escribió Trump en su cuenta de Twitter. Tras la presión del presidente, la agencia ha cedido.
Leave a Comment
You must be logged in to post a comment.

